【JSTnews11月号掲載】NEWS&TOPICS 創発的研究支援事業(FOREST)研究課題「細胞熱工学の深化と生命システム制御」
温度変化をスイッチとしてたんぱく質の機能を操る、新たな分子ツールを開発
2025年11月26日 12時00分更新
細胞内で標的とするたんぱく質の機能を即時に活性化し、細胞の機能を自在に制御する。そんな技術があれば、がん細胞だけを選択的に除去したり、特定の細胞を活性化したりできます。体に負担をかけない治療の実現につながる、重要な技術といえます。最近では、外部から光を照射してたんぱく質の活性を制御する光遺伝学という手法が注目されていますが、生体の組織深部への到達が難しいという課題があります。
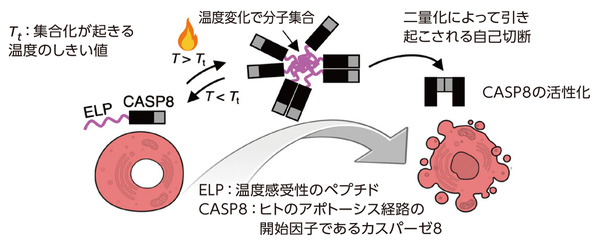
金沢大学ナノ生命科学研究所の新井敏教授らの研究チームは、光に比べて深部まで到達しやすい熱を利用し、温度変化を「スイッチ」として標的たんぱく質の機能を即時に活性化する分子ツールの開発に成功しました。同チームは、生物の状態をより良く保つための「アポトーシス」と呼ばれる細胞死を引き起こす酵素「カスパーゼ8(CASP8)」と、温度上昇により凝集する性質を持つ「エラスチン様ポリペプチド(ELP)」を融合したたんぱく質を合成。ある一定温度を超えると、このたんぱく質が局所的に濃縮してCASP8が活性化されることを利用し、通常の体温下ではCASP8 が機能せず、加熱した時だけ機能してアポトーシスが「オン」になる仕組みを実現しました。さらに、このたんぱく質を用いて、狙った1つの細胞のみを近赤外線レーザーで局所的に加熱し、選択的にアポトーシスを誘導することにも成功しました。
今回の分子ツールは、温度変化に対して大幅には機能が変化しないたんぱく質に、温度に応答する部位を融合することで、温度変化で機能をオン・オフできるようにするものです。医療応用だけでなく、幅広いバイオ分野で役立つでしょう。

この連載の記事
-
第53回
TECH
小さな気泡を発生させて水の摩擦抵抗を減らし、船舶航行の省エネを実現 -
第52回
TECH
深海の極限環境をヒントに、食品製造に欠かせない高機能乳化剤を開発 -
第51回
TECH
産学連携で理想の分析システムを実現! 「超臨界流体クロマトグラフィー」が開く未来の科学 -
第50回
TECH
頭蓋骨をナノマテリアルで代替。生きた脳を超広範囲で観察する手法を完成 -
第49回
TECH
金の原子3つ分の超極細「金量子ニードル」を開発、他分野への応用に期待 -
第47回
TECH
ヒザラガイの硬い「磁鉄鉱の歯」をつくるたんぱく質を発見 -
第46回
TECH
炭化ホウ素ナノ粒子と中性子による新しいがん治療法 -
第45回
TECH
観察とシミュレーションで生命の謎に挑む 発生学と力学の異分野融合 -
第44回
TECH
ゲノム編集技術を産業応用! バイオエコノミー社会のカギとなる“バイオ DX”とは? -
第43回
TECH
北川進博士がノーベル化学賞を受賞 - この連載の一覧へ